МИНИСТЕРСТВО
СЕЛЬСКОГО ХОЗЯЙСТВА
И ПРОДОВОЛЬСТВИЯ
РОССИЙСКОЙ ФЕДЕРАЦИИ
(Минсельхозпрод России)
ДЕПАРТАМЕНТ ВЕТЕРИНАРИИ
17.08.98г. n i3-7-2/-i352
ВРЕМЕННОЕ НАСТАВЛЕНИЕ
по применению набора реагентов
для количественного определения
тироксина в биологических жид-
костях животных методом иммуно-
ферментного анализа ( ИФА-АФ-Т4.)
(В порядке широкого производствен-
ного испытания на 5000 000 иссле-
дований до 2001 года)
1. НАЗНАЧЕНИЕ
В настоящее время для контроля функции щитовидной железы животных
используют диагностикумы,позволяющие определять видонеспецифический
гормон тироксин.
Щитовидная железа продуцирует два специфических тироидных гормона
- трийодтиронин (Тз) и тетрайодтиронин, или тироксин (Т4), а также ти-
реокальцитонин. Основным гормоном железы является тироксин.
Около 70% Т4 связано с тироксинсвязывающим глобулином (ТСГ), 20%
- с тироксинсвязывающим преальбумином ТСПА н 10% - с альбумином.
Период полураспада t4 составляет около недели. Это обусловлено
более прочным, чем у Тз связыванием Т4 с белками. Не связанными с бел-
ками остаются 0,02-0,04% Т4.
Имеются данные, показывающие, что функциональное состояние всех
звеньев гипоталямо-гипофизарно-тиреоидной системы изменяется в за-
висимости от стадии полового цикла и этапа цикла размножения.Уста-
новлена связь между гмпотиреондным состоянием и клиническим прояв-
лением зструса у крупного рогатого скота. Недостаточность функции
щитовидной железы чаще приводит к нарушению полового цикла и ре-
продуктивной способности самок старшего возраста по сравнению с мо-
лодыми. На функциональное состояние щитовидной железы при наруше-
нии репродуктивной функции следует обращать особое внимание еще и
потому, что очень часто скрытый субклннический гипотиреоз сопрово-
ждается патологией воспроизводительной функции у животных и птиц и
снижением лактации у млекопитающих. В пользу роли гипофункцнональ-
ного состояния тиреоидной системы в механизмах нарушения репродуктив-
ной функции свидетельствуют данные об эффективности применения йод-
содержащих препаратов при бесплодии.
Таким образом одной из проблем современной эндокринологии репродук-
ции является проблема оценки тиреоидной системы на разных зтипах
цикла воспроизводства у различных видов животных с целью лечения
и профилактики этих нарушений.
Разработанный набор реагентов предназначен для количественного
определения тироксина в биологических жидкостях животных методом
иммуноферментного анализа.
В основе количественного определения тироксина в биологических
жидкостях животных лежит конкурентный вариант твердофазного иммуно-
ферментного анализа. Принцип метода основан на конкуренции между
адсорбированным на поверхности лунок планшета тироксином и сво-
бодным (в калибровочной пробе или анализируемом образце) тирокси-
ном за активные центры связывания аффинных антител к тироксину,
меченых пероксидазой. В результате иммуноспецифической реакции
между антителами к тироксину и самим тироксином, содержащимся в
пробах (стандарты или образцы) и на поверхности лунок планшета
образуются комплексы антитела-тироксин. Комплекс антиген-антите-
ло, не связанный с поверхностью планшета, удаляют путем промывки.
В результате ферментативной реакции пероксидазы с перекисью водо-
рода субстратного раствора происходит окрашивание 3,3',5,5'-тетраме-
тилбензидина (ТМБ) в синий цвет. Интенсивность окраски обратно про-
порциональна содержанию тироксина в анализируемом образце. Реакцию
останавливают добавлением серной кислоты, вызывающей смену окраски
с синей на ярко желтую. Результаты реакции оцениваются на спек-
трофотометре вертикального сканирования при длине волны 450 нм.
2. ХАРАКТЕРИСТИКА НАБОРА
2.1. Набор расчитан на проведение анализа (5 калибровочных проб,
1 контрольной сыворотки и 42 исследуемых проб в дубликатах на
каждом планшете).
2.2.Состав набора:
1.Планшет 96-луночный с адсорбированным антигеном - 1(2)шт
2.Калиброванные стандарты тироксина, лиофмлизированные
(аморфная масса желтоватого цвета) или жидкие (бесцветная
или желтоватая прозрачная жидкость по 0,5 мл):
а) Стандарт О нМ/л - 1фл.
б) Стандарт 10,0 нМ/л - 1фл.
в) Стандарт 50,0 нМ/л - 1Фл.
г) Стандарт 150,0 нМ/л - 1фл.
д) Стандарт 400,0 нМ/л - 1фл.
е) Контрольная сыворотка, лиофмлмзмрованная -1 фл.
(аморфная масса желтоватого цвета) или жидкая (бесцветная
или желтоватая прозрачная жидкость - 0,5 мл):
3. Конъюгат аффинных антител к тироксину и -1 фл.
пероксидазы из корня хрена ( жидкость красного или
желтоватого цвета - 3 или 6 мл)
4. Буфер для растворения стандартов и контрольной сыворотки - 1фл.
(бесцветная прозрачная жидкость - 5 мл)
5. Буфер для анализа n 1 ( жидкость красного или - 1 фл.
желтоватого цвета - 6 или 12 мл)
6. Буфер для анализа n 2 ( жидкость красного или - 1 фл
желтоватого цвета - 3 или 6 мл)
7. ФСБР - фосфатно-солевой буферный раствор с -1 фл.
детергентом, 20-кратный концентрат (бесцветная
прозрачная жидкость - 25 или 50 мл)
8. 3,3',5,5'- тетраметилбензидин (ТМБ) -1 фл.
(прозрачная жидкость голубоватого цвета -2,2 или 4,4 мл)
9. Субстратный раствор (бесцветная прозрачная жидкость - - 1 фл.
8,8 или 17,6 мл)
10. Стоп-реагент (серная кислота, 2н) - 1 фл.
(бесцветная прозрачная жидкость - 11 или 22 мл)
2.3.Маркировка.
2.3.1. На каждый флакон с компонентом должна быть наклеена этикетка
с указанием: наименования предприятия-изготовителя и его товарного знака,
названия набора, названия реагента, способа подготовки к работе ( для от-
дельных компонентов), условий хранения, срока годности, номера серии, объема
реагента, надписи "Только для "ин витро" диагностики" , содержания тироксина
(для калиброванных стандартов и растворов) .
2.3.2. На каждую коробку должна быть наклеена этикетка с указанием:
наименования предприятия-изготовителя и его товарного знака, "названия набора,
состава набора, надписи "Только для "ин внтро" диагностики", условий хране-
ния, срока годности, номера серии, номера настоящих технических условий. В
коробку вкладывают наставление по применению .
3.ТРАНСПОРТИРОВАНИЕ И ХРАНЕНИЕ
3.1. Транспортирование наборов производят в соответствии с ОСТ 08064-19-07
всеми видами крытого ранспорта при температуре от 2 до 8°С. Допускается
транспортирование наборов при температуре до 25° С в течение 1 сут .
3.2. Наборы хранят при температуре от 2 до 8°С в течении всего
срока годности. Допускается хранение набора при температуре до 25°С не
более 1 сут.
3.3. Срок годности набора - 6 мес. со дня изготовления. Датой изготов-
ления набора считают дату его комплектации.
4. МЕРЫ ПРЕДОСТОРОЖНОСТИ
4.1. При работе с набором следует надевать одноразовые резиновые или
пластиковые перчатки, так как исследуемый материал является потенциально
инфицированным, способным длительное время сохранять и передавать бакт-
ериальные илм вирусные инфекции.
4.2. Химическая посуда и оборудование, которые используются в работе с
набором, должны быть соответствующим образом маркированы и храниться
отдельно.
4.3. Запрещается прием пищи, использование косметических средств и
курение в помещениях, предназначенных для работы с наборами.
5. ПОДГОТОВКА РЕАГЕНТОВ ДЛЯ АНАЛИЗА
5.1. ПРОМЫВОЧНЫЙ БУФЕР
Перед использованием добейтесь полного растворения солей фосфатно-
солевого буферного раствора (ФСБР) путем прогревания флакона в горя-
чей воде. Смешайте необходимое для работы количество ФСБР с дистилли-
рованной водой в следующей пропорции: 1 часть ФСБР + 19 частей дисти-
ллированной воды. Неиспользованный ФСБР храните при 4° С.
5.2. Компоненты набора нельзя оставлять на прямом солнечном свету более
30 мин !!!
5.3. СТАНДАРТЫ ТИРОКСИНА и КОНТРОЛЬНАЯ СЫВОРОТКА
К содержимому флаконов (если стандарты и контрольная сыворотка предс-
тавлены в лиофиллизированном виде) добавьте по 0,5 мл буфера для раство-
рения стандартов и контрольной сыворотки, осторожно перемешайте. Неисполь-
зуемые в работе Стандарты и Контрольную сыворотку храните при + 4° С.
Допустимый срок хранения - 2 месяца.
5.4. КОНЪЮГАТ
Рабочий раствор Конъюгата готовится непосредственно перед использованием
и хранению, в отличие от исходного раствора, не подлежит. Для работы на
целом планшете требуется 10 мл рабочего раствора Конъюгата.
В зависимости от количества анализируемых проб, отберите м смешайте не-
обходимые для проведения анализа количества Буфера для анализа n1,n2 и
Конъюгата в соотношении 2:1:1. Оставшиеся неиспользованными растворы хра-
ните при + 4°С. Допустимый срок хранения - 2 месяца.
5.5. ХРОМОГЕН (ТМВ)
Смешайте содержимое флаконов ТМБ и субстратного раствора в соотношении:
1 часть раствора ТМБ и 4 части субстратного раствора, перемешайте. Для
работы с растворами хромогена необходимо использовать только чистую посу-
ду м чистые наконечники.(Раствор готовится непосредственно перед упот-
реблением). Оставшиеся неиспользованными растворы храните при + 4°С.
6. ПОДГОТОВКА ИССЛЕДУЕМОГО МАТЕРИАЛА
а) сыворотка (плазма)
Из вены животного заберите в центрифужную пробирку 1-3 мл крови и поместите
на 1 час в термостат до образования сгустка. Выдержанные в термостате
образцы отцентрифугируйте при 3000 об/мин в течение 10-15 мин. Отде-
лившуюся сыворотку отберите и используйте в ИФА. Недопустимо использо-
вание гемолизированных и гиперлипидемированных образцов. До проведения
анализа возможно хранение образцов сывороток крови в замороженном состоя-
нии при температуре -20° С.
б) молоко
Пробы молока необходимо брать в одно и то же время дойки. Рекомендуется
отбирать пробы молока вручную в конце основной утренней дойки в объеме
1-1,5 мл. До проведения анализа возможно хранение образцов сывороток кро-
ви в замороженном состоянии при температуре -20° С.
7. ПРОВЕДЕНИЕ АНАЛИЗА
7.1. Порядок маркировки планшета и внесения образцов приведен на схеме.
Время внесения образцов в лунки одного планшета не должно превышать 15 мин.
7.2. Вскрыть упаковку со стрипами (с планшетом) и внести во все исполь-
зуемые для работы лунки по 300 мкл Промывочного буфера.
7.3. Удалите содержимое переворачиванием планшета или отсасыванием так,
чтобы в лунке не осталось жидкости,избегая попадания жидкости в неисполь-
зуемые для работы лункм.
7.4.В лунки ряда А внести по 20 мкл калибровочной пробы,содержащей 0,0
нмоль/л тироксина.
7.5.В лунки ряда В внести по 20 мкл калибровочной пробы, содержащей 10,0
нмоль/л тироксина.
7.6.В лунки ряда С внести по 20 мкл калибровочной пробы, содержащей 50,0
нмоль/л тироксина.
7.7.В лунки ряда d внести по 20 мкл калибровочной пробы, содержащей 150,0
нмоль/л тироксина.
7.8.В лунки Е внести по 20 мкл калибровочной пробы, содержащей 400,0
нмоль/л тироксина.
7.9.В лунки f внести по 20 мкл контрольной сыворотки, содержащей 100,0
нмоль/л тироксина.
7.10.В оставшиеся лунки внести по 20 мкл анализируемых образцов (x)
сыворотки крови.
7.11.Во все лунки планшета внести по 100 мкл раствора конъюгата.
7.12.Планшет закрыть крышкой или клеющей бумагой и инкубировать планшет
в течение 30 минут при температуре + 37° С (желательно в термошейкере).
7.13.После окончания времени инкубации жидкость из лунок удалить перево-
рачиванием планшета, или отсасыванием. Немедленно внести во все лунки
планшета по 300 мкл Промывочного буфера и оставить на 1 минуту, после
чего жидкость из лунок вновь немедленно удалить переворачиванием планше-
та или отсасыванием. Процедуру повторить еще 4 раза. После последней про-
мывки в лунках не должно содержаться жидкости.
СХЕМА ВНЕСЕНИЯ ОБРАЗЦОВ
1 2 3 4
А 0 0 x3 x3
В 10 10 Х4 Х4
С 50 50 Х5 Х5
d 150 150 Х6 Х6
Е 400 400 Х7 Х7
f КС КС Х8 Х8
g Х1 Х1 Х9 Х9
Н Х2 Х2 Х10 Х10
7.14 .Во все лунки планшета внести по 100 мкл раствора хромогена
и инкубировать в течении 7-15 минут при температуре +37 С в термостате .
7.15.Во все лунки планшета внести по 100 мкл стоп-реагента для
остановки ферментативной реакции.
7.16. Измерить оптическую плотность (ОП) всех лунок планшета на
фотометре вертикального сканирования при длине волны 450 нм (при
использовании ТМБ).
8. РАСЧЕТЫ И ГРАФИЧЕСКИЕ ПОСТРОЕНИЯ
Оптическую плотность (ОП) субстратного раствора после остановки
ферментативной реакции измеряют на спектрофотометре типа "Униплан"
или "Унискан" при длине волны 450 нм. Программное обеспечение прибо-
ра позволяет получать результаты измерений в виде графического постро-
ения калибровочной кривой и конечных концентраций тироксина в анали-
зируемых образцах. При использовании приборов с отсутствием програм-
много обеспечения обработки результатов, необходимо провести графичес-
кие построения и расчеты концентраций тироксина вручную. Для этого необ-
ходимо:
а) Вычислить среднее арифметическое значение ОП лунок, содержащих одни
и те же стандарты или пробы: 1А и 2А ;1В и 2В;1С и 2С и т.д.
б) Разделить полученные значения ОП калиброванных стандартов и неиз-
вестных проб ( Вх ) на полученное значение ОП в О стандарте (Во) и умножить
полученные величины на 100% .
в) Построение калибровочной кривой.
Калибровочную кривую строят на полулогарифмической бумаге, откладывая по
оси абсцисс (логарифмическая ) концентрации тироксина (нМ/л), а по оси
ординат (линейная) - полученные значения Вх /Во х 100% в калибровочных
стандартах. Для определения содержания тироксина, в исследуемой пробе
необходимо расчитать величину Вх/Во х100% для данной пробы и по калибро-
вочной кривой установить концентрацию тироксина. Типичная калибровочная
кривая, полученная с использованием набора ИФА-АФ-Т4:
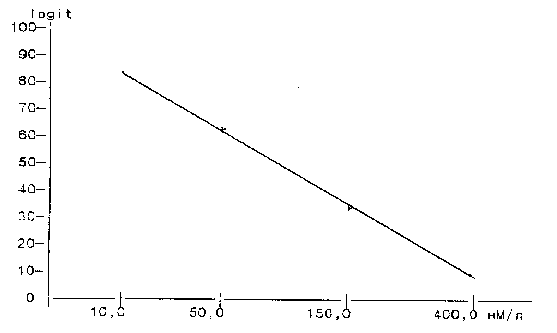 9.АНАЛИТИЧЕСКИЕ ХАРАКТЕРИСТИКИ НАБОРА
9.1. Диапазон измеряемого содержания общего тироксина в сыворотке крови
животных и птиц составляет 10 - 400 нмоль/л.
9.2. Специфичность анализа. Аффинные антитела, используемые в наборе,
дают перекрестную реакцию с 3,3,5-трийодо-l-тиронином (l-t3) -0,06%;
с 3,5-дийодо-l-тирозином - 0,003%.
9.3. Минимальное содержание тироксина, определяемое с помощью набора
ИФА-АФ-Т4., составляет не более 4,0 нмоль/л.
9.4. Тест на "открытие". Данный параметр проверяется путем смешивания
равных объемов контрольной сыворотки м калибровочной пробы, содержащей
50,0 нмоль/л тироксина. Отклонение определяемого содержания тироксина
от рассчитанного находится в пределах 15 % .
9.5. Тест на "линейность". Зависимость содержания тироксина от разве-
дения калибровочных проб находится в диапазоне 85-115 %.
9.6. Воспроизводимость результатов. Коэффициент вариации результатов
измерения содержания тироксина в образцах сыворотки (плазмы) крови
животных, полученных с помощью набора ИФА-АФ-Т4,не превышает 12%.
9.7. Рекомендуется в каждой лаборатории при использовании набора ИФА-АФ-Т4
уточнить значения содержания тироксина, соответствующие нормальным .
9.8. Исключается использование для анализа гемолизированных образцов
сыворотки крови.
10. ДИАГНОСТИЧЕСКАЯ ЦЕННОСТЬ ТЕСТА
Содержание тироксина при нормальных условиях кормления животных в сыво-
ротке (плазме) крови составляет 50-150 нМ/л. Содержание тироксина ниже
40-50 нМ/л свидетельствует о гнпотиреозе, подлежащем лечению. Гипотиреоз
вызывает нарушение репродуктивной способности крупного рогатого скота,
свиноматок, лошадей, домашних животных и птиц. В частности, он является
основной из причин агалактии у свиноматок,крупного рогатого скота и собак,
у птиц гипотиреоз снижает яйценоскость. Одной из часто наблюдаемых при-
чин гипотиреоза у животных является дефицит йода в кормах.
Концентрация тироксина свыше 150-180 нМ/л указывает на гипертмреоз, под-
лежащий лечению.
11. ПОРЯДОК ПРЕДСТАВЛЕНИЯ РЕКЛАМАЦИЙ
Рекламации на наборы реагентов для количественного определения тестос-
терона в биологических жидкостях животных методом иммуноферментного ана-
лиза направляют во Всероссийский государственный научно-исследовательский
институт контроля, стандартизации и сертификации ветеринарных препаратов
(ВГНКИ) (123022, г. Москва, Д-22, Звенигородское шоссе д.5), предпри-
ятию-изготовителю и в Центральную научно-методическую лабораторию (ЦНМВЛ)
(111622,г. Москва, улица Оранжерейная, дом 23) в соответствии с указа-
нием ГУВ Минсельхоза России n 22-7/28 от 08.05.92г."О порядке предъ-
явления рекламаций на ветпрепараты отечественного производства и закупае-
мые по импорту"; одновременно с рекламацией в адрес ВГНКИ направляют одну
тест-систему.
Наставление разработано:
ТОО "М.А.В." (Н.Г. Матрешина, А.В. Матрешин) и Центральной научно-
методической ветеринарной лабораторией (В.А. Седов).
9.АНАЛИТИЧЕСКИЕ ХАРАКТЕРИСТИКИ НАБОРА
9.1. Диапазон измеряемого содержания общего тироксина в сыворотке крови
животных и птиц составляет 10 - 400 нмоль/л.
9.2. Специфичность анализа. Аффинные антитела, используемые в наборе,
дают перекрестную реакцию с 3,3,5-трийодо-l-тиронином (l-t3) -0,06%;
с 3,5-дийодо-l-тирозином - 0,003%.
9.3. Минимальное содержание тироксина, определяемое с помощью набора
ИФА-АФ-Т4., составляет не более 4,0 нмоль/л.
9.4. Тест на "открытие". Данный параметр проверяется путем смешивания
равных объемов контрольной сыворотки м калибровочной пробы, содержащей
50,0 нмоль/л тироксина. Отклонение определяемого содержания тироксина
от рассчитанного находится в пределах 15 % .
9.5. Тест на "линейность". Зависимость содержания тироксина от разве-
дения калибровочных проб находится в диапазоне 85-115 %.
9.6. Воспроизводимость результатов. Коэффициент вариации результатов
измерения содержания тироксина в образцах сыворотки (плазмы) крови
животных, полученных с помощью набора ИФА-АФ-Т4,не превышает 12%.
9.7. Рекомендуется в каждой лаборатории при использовании набора ИФА-АФ-Т4
уточнить значения содержания тироксина, соответствующие нормальным .
9.8. Исключается использование для анализа гемолизированных образцов
сыворотки крови.
10. ДИАГНОСТИЧЕСКАЯ ЦЕННОСТЬ ТЕСТА
Содержание тироксина при нормальных условиях кормления животных в сыво-
ротке (плазме) крови составляет 50-150 нМ/л. Содержание тироксина ниже
40-50 нМ/л свидетельствует о гнпотиреозе, подлежащем лечению. Гипотиреоз
вызывает нарушение репродуктивной способности крупного рогатого скота,
свиноматок, лошадей, домашних животных и птиц. В частности, он является
основной из причин агалактии у свиноматок,крупного рогатого скота и собак,
у птиц гипотиреоз снижает яйценоскость. Одной из часто наблюдаемых при-
чин гипотиреоза у животных является дефицит йода в кормах.
Концентрация тироксина свыше 150-180 нМ/л указывает на гипертмреоз, под-
лежащий лечению.
11. ПОРЯДОК ПРЕДСТАВЛЕНИЯ РЕКЛАМАЦИЙ
Рекламации на наборы реагентов для количественного определения тестос-
терона в биологических жидкостях животных методом иммуноферментного ана-
лиза направляют во Всероссийский государственный научно-исследовательский
институт контроля, стандартизации и сертификации ветеринарных препаратов
(ВГНКИ) (123022, г. Москва, Д-22, Звенигородское шоссе д.5), предпри-
ятию-изготовителю и в Центральную научно-методическую лабораторию (ЦНМВЛ)
(111622,г. Москва, улица Оранжерейная, дом 23) в соответствии с указа-
нием ГУВ Минсельхоза России n 22-7/28 от 08.05.92г."О порядке предъ-
явления рекламаций на ветпрепараты отечественного производства и закупае-
мые по импорту"; одновременно с рекламацией в адрес ВГНКИ направляют одну
тест-систему.
Наставление разработано:
ТОО "М.А.В." (Н.Г. Матрешина, А.В. Матрешин) и Центральной научно-
методической ветеринарной лабораторией (В.А. Седов).
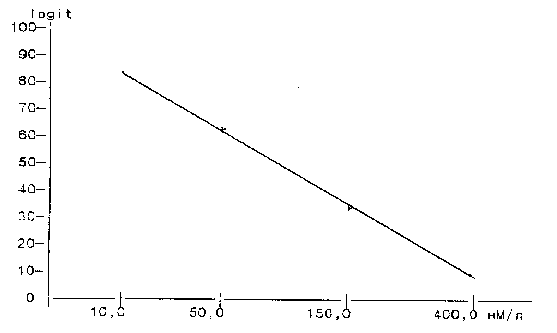 9.АНАЛИТИЧЕСКИЕ ХАРАКТЕРИСТИКИ НАБОРА
9.1. Диапазон измеряемого содержания общего тироксина в сыворотке крови
животных и птиц составляет 10 - 400 нмоль/л.
9.2. Специфичность анализа. Аффинные антитела, используемые в наборе,
дают перекрестную реакцию с 3,3,5-трийодо-l-тиронином (l-t3) -0,06%;
с 3,5-дийодо-l-тирозином - 0,003%.
9.3. Минимальное содержание тироксина, определяемое с помощью набора
ИФА-АФ-Т4., составляет не более 4,0 нмоль/л.
9.4. Тест на "открытие". Данный параметр проверяется путем смешивания
равных объемов контрольной сыворотки м калибровочной пробы, содержащей
50,0 нмоль/л тироксина. Отклонение определяемого содержания тироксина
от рассчитанного находится в пределах 15 % .
9.5. Тест на "линейность". Зависимость содержания тироксина от разве-
дения калибровочных проб находится в диапазоне 85-115 %.
9.6. Воспроизводимость результатов. Коэффициент вариации результатов
измерения содержания тироксина в образцах сыворотки (плазмы) крови
животных, полученных с помощью набора ИФА-АФ-Т4,не превышает 12%.
9.7. Рекомендуется в каждой лаборатории при использовании набора ИФА-АФ-Т4
уточнить значения содержания тироксина, соответствующие нормальным .
9.8. Исключается использование для анализа гемолизированных образцов
сыворотки крови.
10. ДИАГНОСТИЧЕСКАЯ ЦЕННОСТЬ ТЕСТА
Содержание тироксина при нормальных условиях кормления животных в сыво-
ротке (плазме) крови составляет 50-150 нМ/л. Содержание тироксина ниже
40-50 нМ/л свидетельствует о гнпотиреозе, подлежащем лечению. Гипотиреоз
вызывает нарушение репродуктивной способности крупного рогатого скота,
свиноматок, лошадей, домашних животных и птиц. В частности, он является
основной из причин агалактии у свиноматок,крупного рогатого скота и собак,
у птиц гипотиреоз снижает яйценоскость. Одной из часто наблюдаемых при-
чин гипотиреоза у животных является дефицит йода в кормах.
Концентрация тироксина свыше 150-180 нМ/л указывает на гипертмреоз, под-
лежащий лечению.
11. ПОРЯДОК ПРЕДСТАВЛЕНИЯ РЕКЛАМАЦИЙ
Рекламации на наборы реагентов для количественного определения тестос-
терона в биологических жидкостях животных методом иммуноферментного ана-
лиза направляют во Всероссийский государственный научно-исследовательский
институт контроля, стандартизации и сертификации ветеринарных препаратов
(ВГНКИ) (123022, г. Москва, Д-22, Звенигородское шоссе д.5), предпри-
ятию-изготовителю и в Центральную научно-методическую лабораторию (ЦНМВЛ)
(111622,г. Москва, улица Оранжерейная, дом 23) в соответствии с указа-
нием ГУВ Минсельхоза России n 22-7/28 от 08.05.92г."О порядке предъ-
явления рекламаций на ветпрепараты отечественного производства и закупае-
мые по импорту"; одновременно с рекламацией в адрес ВГНКИ направляют одну
тест-систему.
Наставление разработано:
ТОО "М.А.В." (Н.Г. Матрешина, А.В. Матрешин) и Центральной научно-
методической ветеринарной лабораторией (В.А. Седов).
9.АНАЛИТИЧЕСКИЕ ХАРАКТЕРИСТИКИ НАБОРА
9.1. Диапазон измеряемого содержания общего тироксина в сыворотке крови
животных и птиц составляет 10 - 400 нмоль/л.
9.2. Специфичность анализа. Аффинные антитела, используемые в наборе,
дают перекрестную реакцию с 3,3,5-трийодо-l-тиронином (l-t3) -0,06%;
с 3,5-дийодо-l-тирозином - 0,003%.
9.3. Минимальное содержание тироксина, определяемое с помощью набора
ИФА-АФ-Т4., составляет не более 4,0 нмоль/л.
9.4. Тест на "открытие". Данный параметр проверяется путем смешивания
равных объемов контрольной сыворотки м калибровочной пробы, содержащей
50,0 нмоль/л тироксина. Отклонение определяемого содержания тироксина
от рассчитанного находится в пределах 15 % .
9.5. Тест на "линейность". Зависимость содержания тироксина от разве-
дения калибровочных проб находится в диапазоне 85-115 %.
9.6. Воспроизводимость результатов. Коэффициент вариации результатов
измерения содержания тироксина в образцах сыворотки (плазмы) крови
животных, полученных с помощью набора ИФА-АФ-Т4,не превышает 12%.
9.7. Рекомендуется в каждой лаборатории при использовании набора ИФА-АФ-Т4
уточнить значения содержания тироксина, соответствующие нормальным .
9.8. Исключается использование для анализа гемолизированных образцов
сыворотки крови.
10. ДИАГНОСТИЧЕСКАЯ ЦЕННОСТЬ ТЕСТА
Содержание тироксина при нормальных условиях кормления животных в сыво-
ротке (плазме) крови составляет 50-150 нМ/л. Содержание тироксина ниже
40-50 нМ/л свидетельствует о гнпотиреозе, подлежащем лечению. Гипотиреоз
вызывает нарушение репродуктивной способности крупного рогатого скота,
свиноматок, лошадей, домашних животных и птиц. В частности, он является
основной из причин агалактии у свиноматок,крупного рогатого скота и собак,
у птиц гипотиреоз снижает яйценоскость. Одной из часто наблюдаемых при-
чин гипотиреоза у животных является дефицит йода в кормах.
Концентрация тироксина свыше 150-180 нМ/л указывает на гипертмреоз, под-
лежащий лечению.
11. ПОРЯДОК ПРЕДСТАВЛЕНИЯ РЕКЛАМАЦИЙ
Рекламации на наборы реагентов для количественного определения тестос-
терона в биологических жидкостях животных методом иммуноферментного ана-
лиза направляют во Всероссийский государственный научно-исследовательский
институт контроля, стандартизации и сертификации ветеринарных препаратов
(ВГНКИ) (123022, г. Москва, Д-22, Звенигородское шоссе д.5), предпри-
ятию-изготовителю и в Центральную научно-методическую лабораторию (ЦНМВЛ)
(111622,г. Москва, улица Оранжерейная, дом 23) в соответствии с указа-
нием ГУВ Минсельхоза России n 22-7/28 от 08.05.92г."О порядке предъ-
явления рекламаций на ветпрепараты отечественного производства и закупае-
мые по импорту"; одновременно с рекламацией в адрес ВГНКИ направляют одну
тест-систему.
Наставление разработано:
ТОО "М.А.В." (Н.Г. Матрешина, А.В. Матрешин) и Центральной научно-
методической ветеринарной лабораторией (В.А. Седов).