МИНИСТЕРСТВО
СЕЛЬСКОГО ХОЗЯЙСТВА
И ПРОДОВОЛЬСТВИЯ
РОССИЙСКОЙ ФЕДЕРАЦИИ
(Минсельхозпрод России)
ДЕПАРТАМЕНТ ВЕТЕРИНАРИИ
17.08.98г. 13-7-2/1361
ВРЕМЕННОЕ НАСТАВЛЕНИЕ
по применению набора реагентов для коли-
чественного определения эстрадиола 17-бета в
продуктах животного происхождения методом
иммуноферментного анализа ( ИФА-АФ-ЭСТР.)
(В порядке широкого производственного ис-
пытания на 1000 000 исследований до 2001г.)
1. НАЗНАЧЕНИЕ
Контроль качества продуктов животного происхождения ветеринарной
службой является одним из важнейших профилактических мероприятий по
сохранению здоровья нации. При оценке качества продуктов питания жи-
вотного происхождения, одним из важнейших показателей является конт-
роль уровня стероидных гормонов - мощнейших регуляторов обмена веществ
в организме.
Причиной этого является их способность длительное время сохра-
няться в замороженных продуктах животного происхождения, выдерживать
термическую обработку и свободно всасываться из содержимого желудоч-
но-кишечного тракта. Стерондные гормоны не обладают видовой специфич-
ностью, поэтому, попадая в организм человека, они активно вмешиваются
в межгормональные взаимоотношения, нарушая тем самым присущий данному
организму обмен веществ, влияя на проявление половых признаков и поло-
вую функцию организма.
В современном промышленном животноводстве, птицеводстве и рыбо-
водстве при интенсивных технологиях выращивания животных, в нарушение
технологических регламентов, часто прибегают к незаконному использова-
нию гормональных стимуляторов роста. Использование препаратов данного
класса строго контролируется в развитых странах уполномоченными орга-
нами государственного надзора. Для зтого в мировой практике активно
используют экспресс-методы контроля безопасности пищевых продуктов,
среди которых лидирующее положение занял иммуноферментный метод анали-
за. В США и некоторых странах ЕЭС методы мммуноферментного анализа
продуктов животного происхождения доведены до статуса национальных
стандартов.
В России из-за отсутствия эффективных, высокопроизводительных и
простых в исполнении методов количественного определения стероидных
гормонов до настоящего времени не осуществлялся эффективный контроль
за содержанием гормональных препаратов в целом перечне продуктов жи-
вотного происхождения, как отечественного, так и, в особенности, им-
портного производства.
ПЕРЕЧЕНЬ ПРОДУКТОВ ЖИВОТНОГО ПРОИСХОЖДЕНИЯ, ПОДЛЕЖАЩИХ
ИССЛЕДОВАНИЮ НА СОДЕРЖАНИЕ ЭСТРАДИОЛА-17бета.
1. Мясо : свежее, охлажденное и мороженое конины, говядины, сви-
нины, баранины, козлятины, кролика, мясо других видов, блоки, мясные
полуфабрикаты.
2. Мясо птицы: свежее, охлажденное и мороженое кур, уток, гусей,
индеек, перепелов, индеек тяжелых кроссов.
3. Колбасы и кулинарные изделия из мяса (говядины, свинины, бара-
нины, конины, субпродуктов) и птицы: колбасы сырокопченые, колбасы по-
лукопченые, колбасы варено-копченые, колбасы вареные, сосиски, сар-
дельки, колбасы и колбаски вареные для школьного питания из мяса и
птицы, колбасы ливерные, колбасы кровяные, зельцы, паштеты, студни,
соусы, мясные вареные, жареные,запеченные и копчено-запеченные продук-
ты .
4. Консервы из мяса и птицы, консервы мясо-растительные.
5. Субпродукты сельскохозяйственных животных и птиц.
6. Полуфабрикаты.
7. Масло коровье, жиры животные.
8. Яйца и изделия пищевые на яичной основе.
9. Рыба и рыбопродукты, рыбные консервы.
10. Молоко, сливки, кисломолочные изделия, консервы молочные, мо-
локо м молочные изделия сухие, сыры и творожные изделия, мороженое.
Разработанный ИфА-метод предназначен для решения проблемы массо-
вого рутинного контроля за содержанием зстрадмола-17бета, в том числе и
на продуктовых рынках.
В основе количественного определения зстрадмола-17бета в продуктах
животного происхождения лежит конкурентный вариант таердофазного имму-
ноферментного анализа. Принцип метода основан на конкуренции между ад-
сорбированным на поверхности лунок планшета зстрадиолом-17бета и свобод-
ным (в калибровочной пробе или анализируемом образце) зстрадиолом- 17бета
за активные центры связывания аффинных антител к зстрадиолу-17бета, ме-
ченых пероксидазой. В результате иммуноспецифической реакции между ан-
тителами к зстрадиолу-17бета и самим зстрадиолом- 17бета , содержащимся в
пробах (стандарты или образцы) и на поверхности лунок планшета образу-
ются комплексы антитела-зстрадиол- 17бета . Комплекс антиген-антитело, не
связанный с поверхностью планшета, удаляют путем промывки.
В результате ферментативной реакции пероксидазы с перекисью водо-
рода субстратного раствора происходит окрашивание 3,3',5,5'- тетраме-
тилбензидина (ТМБ) в синий цвет. Интенсивность окраски обратно пропор-
циональна содержанию зстрадиола-17бета в анализируемом образце. Реакцию
останавливают добавлением серной кислоты, вызывающем смену окраски с
синей на ярко желтую. Результаты реакции оцениваются на спектрофото-
метре вертнкального сканирования при длине волны 450 нм.
2. ХАРАКТЕРИСТИКА НАБОРА
2.1. Набор расчитан на проведение анализа (6 калибровочных проб и
14 неизвестных проб в дубликатах на каждом планшете).
2.2.Состав набора:
1.Планшет 96-луночный с адсорбированным антигеном - 1(2)шт.
2.Калиброванные стандарты зстраднола-17бета (бесцветная или
желтоватая прозрачная жидкость по 0,5 мл):
а) Стандарт 0 нг/мл - 1 фл.
б) Стандарт 0,1 нг/мл - 1 фл.
в) Стандарт 0,3 нг/мп - 1 фл.
г) Стандарт 1,0 нг/мл - 1 фл.
д) Стандарт 3,0 нг/мп - 1 Фл.
е) Стандарт 10,0 нг/мл - 1 фл.
3. Конъюгат аффинных антител к зстрадмолу-17бета и - 1 фл.
пероксидазы из корня хрена ( жидкость красного или
желтоватого цвета - 1,5 или 3 мл)
4. Калиброванный раствор зстрадиола-17бета - 400 мкг/мл - 1 фл.
(бесцветная или желтоватая прозрачная жидкость - 3 или 6 мл)
5. Калиброванный раствор зстрадиола-17бета- 400 нг/мл) - 1 фл.
(бесцветная или желтоватая прозрачная жидкость(3 мл)
6. Растворитель для анализируемых проб - 1 фл.
(бесцветная прозрачная жидкость - 30 или 60 мл)
7. Буфер для анализа n 1 ( жидкость красного или - 1 фл.
желтоватого цвета - 3 или 6 мл)
8. Буфер для анализа n 2 ( жидкость красного или - 1 фл
желтоватого цвета - 1,5 или 3 мл)
9. ФСБР - фосфатно-солевой буферный раствор с - 1 фл.
детергентом, 20-кратный концентрат (бесцветная прозрачная
жидкость - 25 или 50 мл)
10. 3,3',5,5'- тетраметилбензидмн (ТМБ) - 1 фл.
(прозрачная жидкость голубоватого цвета -2,2 или 4,4 мл)
11. Субстратный раствор (бесцветная прозрачная жидкость - - 1 фл.
8,8 или 17,6 мл)
12. Стоп-реагент (серная кислота, 2н) - 1 фл.
(бесцветная прозрачная жидкость - 11 или 22 мл)
2.3.Маркировка.
2.3.1. На каждый флакон с компонентом должна быть наклеена эти-
кетка с указанием: наименования предприятия-изготовителя и его товар-
ного знака, названия набора, названия реагента, способа подготовки к
работе ( для отдельных компонентов), условий хранения, срока годности,
номера серии, объема реагента, надписи "Только для "ин витро" диагнос-
тики", содержания зстрадиола-17бета (для калиброванных стандартов и
растворов).
2.3.2. На каждую коробку должна быть наклеена этикетка с указани-
ем: наименования предприятия-изготовителя и его товарного знака, наз-
вания набора, состава набора, надписи "Только для "ин витро" диагнос-
тики", условий хранения, срока годности, номера серии, номера настоя-
щих технических условий. В коробку вкладывают наставление по примене-
нию.
3.ТРАНСПОРТИРОВАНИЕ И ХРАНЕНИЕ
3.1. Транспортирование наборов производят в соответствии с ОСТ
08064-19-07 всеми видами крытого транспорта при температуре от 2 до 8° С.
Допускается транспортирование наборов при температуре до 25° С в
течение 1 сут.
3.2. Наборы хранят при температуре от 2 до 8° С в течении всего
срока годности. Допускается хранение набора при температуре до 25° С
не более 1 сут.
3.3. Срок годности набора - 5 мес. со дня изготовления.
Датой изготовления набора считают дату его комплектации.
4. МЕРЫ ПРЕДОСТОРОЖНОСТИ
4.1. При работе с набором следует надевать одноразовые резиновые
или пластиковые перчатки, так как исследуемый материал является потен-
циально инфицированным, способным длительное время сохранять и переда-
вать бактериальные или вирусные инфекции.
4.2. Химическая посуда и оборудование, которые используются в ра-
боте с набором, должны быть соответствующим образом маркированы и хра-
ниться отдельно.
4.3. Запрещается прием пищи, использование косметических средств
и курение в помещениях, предназначенных для работы с наборами.
5. ПОДГОТОВКА РЕАГЕНТОВ ДЛЯ АНАЛИЗА
5.1. Промывочный буфер
Перед использованием добейтесь полного растворения солей фосфат-
но-солевого буферного раствора (ФСБР) путем прогревания флакона в го-
рячей воде. Смешайте необходимое для работы количество ФСБР с дистил-
лированной водой в следующей пропорции: 1 часть ФСВР + 19 частей дис-
тиллированной воды. Неиспользованный ФСБР храните при +4°С.
5.2. КОНЪЮГАТ
Рабочий раствор Конъюгата готовится непосредственно перед использо-
ванием и хранению, в отличие от исходного раствора, не подлежит.
Для работы на целом планшете требуется 5 мл рабочего раствора Конъ-
югата. В зависимости от количества анализируемых проб, смешайте Буфер
для анализа n1, Буфер для анализа n2 и Конъюгат в соотношении 2:1:1.
Оставшиеся не использованными исходные растворы Конъюгата и Буфера для
анализа n1 и n2 храните при + 4° С.
5.3. СТАНДАРТЫ И КАЛИБРОВАННЫЕ РАСТВОРЫ
Перед использованием стандарты, калиброванные растворы и раствори-
тель для анализируемых проб следует прогреть для размораживания раст-
ворителя. Чистыми наконечниками перенесите по 60 мкл каждого стандарта
и анализируемого образца в предварительно маркированные флаконы и до-
бавьте по 390 мкл Промывочного буфера, перемешайте и используйте в
ИФА. Исходные растворы храните при +4° С.
5.4. ХРОМОГЕН
Смешайте содержимое флаконов ТМБ и субстратного раствора в соотноше-
нии: 1 часть раствора ТМВ и 4 части субстратного раствора, переме-
шайте. Для работы с растворами хромогена необходимо использовать толь-
ко чистую посуду и чистые наконечники.(Раствор готовится непосредс-
твенно перед употреблением). Оставшиеся неиспользованными растворы
храните при + 4°С.
6.ПОДГОТОВКА ИССЛЕДУЕМОГО МАТЕРИАЛА
Для определения истинной концентрации гормонов в каждом исследуе-
мом образце необходимо оценить процент выхода дополнительно вносимых
стероидов. Для этого каждый образец пробы исследуется как в чистом ви-
де, так и с добавкой определяемого гормона. Во всех случаях, для ана-
лиза 1 исследуемой пробы, необходимо одновременно исследовать 2 пробы
того же образца с добавками калиброванных растворов зстрадиола-17бета,
вносимых внутрь образца до гомогенизации (экстракции) и после экстрак-
ции .
Все работы по экстракции исследуемых образцов необходимо прово-
дить в вытяжном шкафу.
Продукты из мяса. птицы, рыбы. сыр. творог.
1. Берется усредненная навеска из разных мест исследуемого образ-
ца массой 40 г, которая делится на 2 части по 20 г каждая. В одну из
частей вносится 20 мкл калиброванного раствора зстрадмола, содержащего
5 мкг/мл гормона для оценки эффективности экстракционной процедуры.
2. Исследуемые пробы тщательно гомогенизируются до мелкодисперс-
ного состояния в 40 мл 0,1 n раствора соляной кислоты каждая.
3. По 3 г полученных гомогенатов переносят в полиэтиленовые про-
бирки и добавляют тройной по отношению к гомогенату объем диэтилового
эфира (9 мл), плотно закрывают крышками, тщательно встряхивают в тече-
ние 5-10 минут и выдерживают в морозильной камере или сухом льде до
замерзания водной (нижней) фазы.
4.Прозрачную эфирную фазу каждого образца аккуратно сливают в
пенициллиновые флаконы и выпаривают досуха на водяной бане с темпера-
турой воды +37° С в вытяжном шкафу (необходимо следить, чтобы эфир не
выплескивался).
5. К прогретым (+56° С) сухим остаткам экстрактов добавляют по 1
мл растворителя для анализируемых проб. Пробы тщательно перемешивают в
течение 2-3 минут и охлаждают 15 минут при +4° С.
6. Очистка образцов от жира производится путем фильтрации через
бумажные фильтры.
7. Пронумеруйте 3 чистых флакона: 1- Х1; 2- y1; 3- z1.
- в 1-й внесите 60 мкл фильтрата, полученного после экстракции
нативного анализируемого образца (x1);
- во 2-й внесите 60 мкл фильтрата анализируемого образца с добав-
кой гормона, внесенного до экстракции (y1) ;
- в 3-й (z1) внесите 60 мкл фильтрата, полученного после экстрак-
ции нативного анализируемого образца (x1); сюда же добавьте 60 мкл ка-
либрованного раствора зстрадиола, содержащего 5 нг/мл гормона ;
- в 1 и 2 флаконы внесите по 390 мкл Промывочного буфера, в 3-й
внесите 330 мкл Промывочного буфера, осторожно встряхните флаконы и
используйте растворы в ИФА.
Жиры животного происхождения
1. Берется усредненная навеска из разных мест исследуемого образ-
ца массой 40 г, которая делится на 2 части по 20 г каждая. Пробы меха-
нически измельчаются и растапливаются. В одну из частей вносится 200
мкл калиброванного раствора исследуемого стероида (5 мкг/мл) для
оценки эффективности экстракционной процедуры. Пробы тщательно встря-
хиваются .
2. По 200 мг полученных подогретых до жидкого состояния гомогена-
тов переносят пипеткой в полиэтиленовые пробирки и добавляют по 2 мл
дизтилового эфира, плотно закрывают крышками, тщательно встряхивают в
течение 5-10 минут и выдерживают в морозильной камере или сухом льде
до замерзания водной (нижней) фазы.
3.Прозрачную эфирную фазу каждого образца сливают в пеницмллино-
вые флаконы м выпаривают досуха на водяной бане с температурой воды
+37°С в вытяжном шкафу (необходимо следить, чтобы эфир не выплески-
вался ) .
4. К прогретым (+56° С) сухим остаткам экстрактов добавляют по 2
мл растворителя для анализируемых проб, пробы тщательно перемешивают в
течение 2-3 минут и охлаждают 15 минут при +4° С.
5. Очистка образцов от жира производится путем фильтрации через
бумажные фильтры, фильтраты используются в ИФА.
6. Пронумеруйте 3 чистых флакона: 1- x1; 2- y1; 3- z1.
- в 1-й внесите 60 мкл фильтрата, полученного после экстракции
нативного анализируемого образца (x1);
- во 2-й внесите 60 мкл фильтрата анализируемого образца с добав-
кой гормона, внесенного до экстракции (y1) ;
- в 3-й (z1) внесите 60 мкл фильтрата, полученного после экстрак-
ции нативного анализируемого образца (x1); сюда же добавьте 60 мкл ка-
либрованного раствора зстрадиола, содержащего 5 нг/мл гормона ;
- в 1 и 2 флаконы внесите по 390 мкл Промывочного буфера, в 3-й
внесите 330 мкл Промывочного буфера, осторожно встряхните флаконы и
используйте растворы в ИФА.
Молоко и кисломолочные продукты
1. Берутся в стеклянные виалы 2 навески образцов массой по 60 г
(мл) каждая, прогреваются при +37°С в течение 30 минут. В одну навес-
ку вносится 20 мкл калиброванного раствора зстрадиола (5 мкг/мл) для
оценки эффективности экстракционной процедуры. Пробы тщательно встря-
хиваются .
2. По 3 г(мл) полученных гомогенатов переносят в полиэтиленовые
пробирки и добавляют тройной по отношению к гомогенату объем дизтило-
вого эфира (9 мл), плотно закрывают крышками, тщательно встряхивают в
течение 5-10 минут и центрифугируют в течение 15 минут при ЗОООg, а
затем выдерживают в морозильной камере или сухом льде до замерзания
водной (нижней) фазы.
3.Прозрачную эфирную фазу каждого образца аккуратно сливают в
пеннциллиновые флаконы и выпаривают досуха на водяной бане с темпера-
турой воды +37° С в вытяжном шкафу (необходимо следить, чтобы эфир не
выплескивался) .
4. К прогретым (+56° С) сухим остаткам экстрактов добавляют по 1
мл растворителя для анализируемых проб. Пробы тщательно перемешивают в
течение 2-3 минут и охлаждают 15 минут при +4° С.
5. Очистка образцов от жира производится путем фильтрации через
бумажные фильтры, фильтраты используются в ИФА.
6. Пронумеруйте 3 чистых флакона: 1- x1; 2- y1; 3- z1.
- в 1-й внесите 60 мкл фильтрата, полученного после экстракции
нативного анализируемого образца (x1);
- во 2-й внесите 60 мкл фильтрата анализируемого образца с добав-
кой гормона, внесенного до экстракции (y1) ;
- в 3-й (z1) внесите 60 мкл фильтрата, полученного после зкстрак-
ии нативного анализируемого образца (x1); сюда же добавьте 60 мкл ка-
либрованного раствора эстрадиола, содержащего 5 нг/мл гормона ;
- в 1 и 2 флаконы внесите по 390 мкл Промывочного буфера, в 3-й
внесите 330 мкл Промывочного буфера, осторожно встряхните флаконы и
используйте в ИФА.
7. ПРОВЕДЕНИЕ АНАЛИЗА
7.1. Порядок маркировки планшета и внесения образцов приведен на
схеме. Время внесения образцов в лунки одного планшета не должно пре-
вышать 15 мин.
7.2. Вскрыть упаковку со стрипами (с планшетом) и внести во все
используемые для работы лунки по 300 мкл Промывочного буфера.
7.3. Удалите содержимое переворачиванием планшета или отсасывани-
ем так, чтобы в лунке не осталось жидкости.
7.4. В лунки 1,2 ряда А внести по 150 мкл калибровочной пробы,
содержащей Стандарт О нг/мл.
7.5. В лунки 1,2 ряда В внести по 150 мкл калибровочной пробы,
содержащей Стандарт 0,1 нг/мл.
7.6.В лунки 1,2 ряд 6 С внести по 150 мкл калибровочной пробы, со-
держащей Стандарт 0,3 нг/мл.
7.7. В лунки 1,2 ряда d внести по 150 мкл калибровочной пробы,
содержащей Стандарт 1,0 нг/мл.
7.8. В лунки 1,2 ряда Е внести по 150 мкл калибровочной пробы, со-
держащей Стандарт 3,0 нг/мл.
7.9. В лунки 1,2 ряда f внести по 150 мкл калибровочной пробы,
содержащей Стандарт 10,0 нг/мл.
7.10.В лункм 1,2 ряда g внести по 150 мкл образца из флакона x1.
7.11.В лунки 1,2 ряда Н внести по 150 мкл образца из флакона y1.
7.12.В лунки 3,4 ряда А внести по 150 мкл образца из флакона z1.
7.13. Во все используемые лунки планшета внести по 50 мкл раство-
ра Конъгогата.
7.14. Планшет закрыть крышкой или клеющей бумагой и инкубировать
планшет в течение 30 минут в вибротермостате при температуре +37° С.
7.15. После окончания времени инкубации жидкость из лунок удалить
переворачиванием планшета или отсасыванием. Немедленно внести во все
лунки планшета по 300 мкл Промывочного буфера,после чего жидкость из
лунок вновь немедленно удалить переворачиванием планшета или отсасыва-
нием. Процедуру повторить еще 4 раза. После последней промывки в лун-
ках не должно содержаться жидкости.
7.16. Во все используемые лунки планшета внести по 100 мкл раст-
вора Хромогена и инкубировать в течении 7-15 минут при температуре
+37° С в термостате.
7.17. Во все используемые лунки планшета к раствору Хромогена до-
бавить по 100 мкл Стоп-реагента для остановки ферментативной реакции.
Окраска стабильна в течении 30 минут.
7.18. Измерить оптическую плотность (ОП) всех лунок планшета на
фотометре вертикального сканирования при длине волны 450 нм не позднее
30 минут после остановки ферментативной реакции.
СХЕМА ВНЕСЕНИЯ ОБРАЗЦОВ
1 2 3 4
А Стандарт 0 Стандарт 0 z1 z1
В Стандарт 0,1 Стандарт 0,1 x2 x2
С Стандарт 0,3 Стандарт 0,3 y2 y2
d Стандарт 1,0 Стандарт 1,0 z2 z2
Е Стандарт 3,0 Стандарт 3,0 Хз Хз
f Стандарт 10,0 Стандарт 10,0 yз yз
g x1 x1 zз z3
Н y1 y1 x. . . x. . .
и т.д
8. РАСЧЕТЫ И ГРАФИЧЕСКИЕ ПОСТРОЕНИЯ
Оптическую плотность (ОП) субстратного раствора после остановки
ферментативной реакции измеряют на спектрофотометре " Униплан" произ-
водства ЗАО " ПИКОН" или на иммуноферментном оборудовании аналогичного
класса при длине волны 450 нм. Программное обеспечение прибора позво-
ляет получать результаты измерений в виде графического построения ка-
либровочной кривой и конечных концентраций зстрадиола-17бета в анализиру-
емых образцах. При использовании приборов с отсутствием программного
обеспечения обработки результатов, необходимо провести графические
построения и расчеты концентраций эстрадиола-17бета вручную. Для этого
необходимо:
а) Вычислить среднее арифметическое значение ОП лунок, содержащих
одни и те же стандарты или пробы: 1А и 2А ;1В и 2В;1С и 2С и т.д.
б) Разделить полученные значения ОП калиброванных стандартов и
неизвестных проб ( Вх ) на полученное значение ОП в О стандарте ( Во)
и умножить полученные величины на 100% .
в) Построение калибровочной кривой.
Калибровочную кривую строят на полулогарифмической бумаге, откла-
дывая по оси абсцисс (логарифмическая) концентрации зстрадиола-17бета
(нг/мл), а по оси ординат (линейная) - полученные значения Вх /Во х
100% в калибровочных стандартах. Для определения содержания зстрадио-
ла 17бета, в исследуемой пробе необходимо расчитать величину Вх/Во х100%
для данной пробы и по калибровочной кривой установить концентрацию
зстрадиола-17бета.
Типичная калибровочная кривая, полученная с использованием набора
ИФА-АФ-Эстр. представлена на рис.
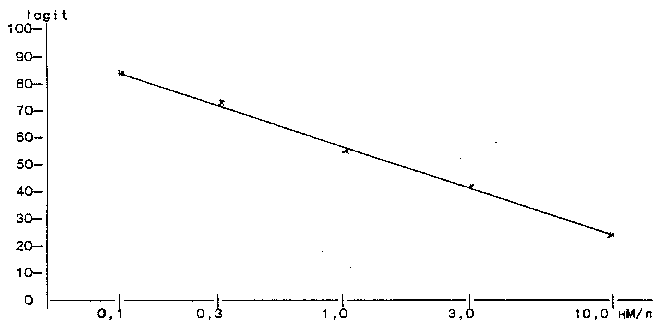 г). Расчет коэффициента выхода гормона (Кв)
Расчет проводится после определения конечных концентраций зстра-
диола-17бета в анализируемых образцах x,y,z (в нг/мл).
y - Х
Кв= ------
z - Х
д). Расчет коэффициента неспецифического влияния компонентов ана-
лизируемых проб на специфическую реакцию связывания зстрадиола-17бета ан-
тителами .
z(нг/мл)
Кнесп. ---------------
5 (нг/мл) + Х
Если Кнесп.> 1 , то это свидетельствует о наличии в образцах сте-
роидов или других соединений, ингибирующих специфическую реакцию.
ПРОДУКТЫ ЖИВОТНОГО ПРОИСХОЖДЕНИЯ, У КОТОРЫХ ЗНАЧЕНИЕ Кнесп ПРЕВЫ-
ШАЕТ 1,15 НЕ РЕКОМЕНДУЕТСЯ УПОТРЕБЛЯТЬ В ПИЩУ ДО ИДЕНТИФИКАЦИИ ОБНАРУ-
ЖЕННЫХ СОЕДИНЕНИЙ; ПРИ ЭТОМ НЕОБХОДИМО ИСКЛЮЧИТЬ НАЛИЧИЕ СТИЛЬБЕНОВ
(ДИЭТИЛСТИЛЬБЭСТРОЛА, ГЕКСОЭСТРОЛА, ДИЕНОЭСТРОЛА) И АНАБОЛИЧЕСКИХ СТЕ-
РОИДОВ (ТРЕНБОЛОНА И 19-НОРТЕСТОСТЕРОНА) В АНАЛИЗИРУЕМЫХ ОБРАЗЦАХ.
е). Расчет истинной концентрации гормона в анализируемом образце
(нг/мл):
Х
Кист. =------------
Кв х К н е с п .
ж). Расчет истинной концентрации гормона в 1 килограмме анализиру-
емого образца (мг/кг):
- Концентрация зстрадиола-17бета в мг/кг мясных продуктов, творога,
сыра расчитывается путем деления полученной величины Кист на 1000.
- Концентрация зстрадиола-17бета в мг/кг масла и жиров животного
происхождения расчитывается путем деления полученной величины Кист на
100.
- Концентрация зстрадиола-17бета в мг/кг молока и кисломолочных про-
дуктов расчитывается путем деления полученной величины Кист на 3000.
ДОПУСТИМЫЕ УРОВНИ ЭСТРАДИОЛА- 17бета
Для всех вышеперечисленных продуктов, за исключением масла ко-
ровьего, допускается уровень зстрадиола-17бета не более 0.0005 мг/кг
(для масла допускается содержание зстрадиола-17бета не более 0,015 мг/кг.
В случае превышения уровня эстрадиола-17бетта в анализируемом образце бо-
лее,чем на 15%, данный продукт не рекомендуется к употреблению в пищу.
9.АНАЛИТИЧЕСКИЕ ХАРАКТЕРИСТИКИ НАБОРА
9.1. Диапазон измеряемого содержания зстрадиола-17бета составляет
0,1 - 10,0 нг/мл.
9.2. Специфичность анализа. Перекрестная реакция антисыворотки к
зстрадиолу-17бета со структурно-родственными стероидами приведена в таблице 2
Таблица 2
Стероид Перекрестная реакция,%
Эстрадиол-17бета 100
Эстрон 12,0
Эстриол 1,2
Кортизол <0,01
Тестостерон <0,01
5a-Дигидротестостерон <0,01
Прогестерон <0,01
9.3. Минимальное содержание зстрадиола-17бета , определяемое с по-
мощью набора ИФА-АФ- Эстр., составляет 0,06 нг/мл.
9.4. Тест на "линейность". Зависимость содержания зстраднола-17бета
от разведения калибровочных проб находится в диапазоне 85-115 %.
9.5. Воспроизводимость результатов. Коэффициент вариации резуль-
татов измерения содержания зстрадиола-17бета в образцах,полученных с по-
мощью набора ИфА-АФ-Эстр., не превышает 12 %.
9.5. Рекомендуется в каждой лаборатории при использовании набора
ИфА-АФ-Эстр.уточнить значения содержания зстрадиола-17бета, соответствую-
щие нормальным.
10. ПОРЯДОК ПРЕДСТАВЛЕНИЯ РЕКЛАМАЦИЙ
Рекламации на наборы реагентов для количественного определения
зстрадиола в продуктах животного происхождения методом иммунофермент-
ного анализа направляют во Всероссийский государственный научно-иссле-
довательский институт контроля, стандартизации и сертификации ветери-
ных препаратов (ВГНКИ) (123022, г. Москва, Д-22, Звенигородское шоссе,
д.5), предприятию-изготовителю и в Центральную научно-методическую ла-
бораторию (ЦНМВЛ) (111522,г. Москва, улица Оранжерейная, дом 23) в со-
ответствии с указанием ГУБ Минсельхоза России n 22-7/28 от 08.05.92 г.
О порядке предъявления рекламаций на ветпрепараты отечественного
производства и закупаемые по импорту"; одновременно с рекламацией в
адрес ВГНКИ направляют одну тест-систему.
Наставление разработано:
ТОО "М.А.В." (Н.Г.Матрешмна, А.В.Матрешин) и Центральной науч-
но-методической ветеринарной лабораторией (В.А. Седов).
г). Расчет коэффициента выхода гормона (Кв)
Расчет проводится после определения конечных концентраций зстра-
диола-17бета в анализируемых образцах x,y,z (в нг/мл).
y - Х
Кв= ------
z - Х
д). Расчет коэффициента неспецифического влияния компонентов ана-
лизируемых проб на специфическую реакцию связывания зстрадиола-17бета ан-
тителами .
z(нг/мл)
Кнесп. ---------------
5 (нг/мл) + Х
Если Кнесп.> 1 , то это свидетельствует о наличии в образцах сте-
роидов или других соединений, ингибирующих специфическую реакцию.
ПРОДУКТЫ ЖИВОТНОГО ПРОИСХОЖДЕНИЯ, У КОТОРЫХ ЗНАЧЕНИЕ Кнесп ПРЕВЫ-
ШАЕТ 1,15 НЕ РЕКОМЕНДУЕТСЯ УПОТРЕБЛЯТЬ В ПИЩУ ДО ИДЕНТИФИКАЦИИ ОБНАРУ-
ЖЕННЫХ СОЕДИНЕНИЙ; ПРИ ЭТОМ НЕОБХОДИМО ИСКЛЮЧИТЬ НАЛИЧИЕ СТИЛЬБЕНОВ
(ДИЭТИЛСТИЛЬБЭСТРОЛА, ГЕКСОЭСТРОЛА, ДИЕНОЭСТРОЛА) И АНАБОЛИЧЕСКИХ СТЕ-
РОИДОВ (ТРЕНБОЛОНА И 19-НОРТЕСТОСТЕРОНА) В АНАЛИЗИРУЕМЫХ ОБРАЗЦАХ.
е). Расчет истинной концентрации гормона в анализируемом образце
(нг/мл):
Х
Кист. =------------
Кв х К н е с п .
ж). Расчет истинной концентрации гормона в 1 килограмме анализиру-
емого образца (мг/кг):
- Концентрация зстрадиола-17бета в мг/кг мясных продуктов, творога,
сыра расчитывается путем деления полученной величины Кист на 1000.
- Концентрация зстрадиола-17бета в мг/кг масла и жиров животного
происхождения расчитывается путем деления полученной величины Кист на
100.
- Концентрация зстрадиола-17бета в мг/кг молока и кисломолочных про-
дуктов расчитывается путем деления полученной величины Кист на 3000.
ДОПУСТИМЫЕ УРОВНИ ЭСТРАДИОЛА- 17бета
Для всех вышеперечисленных продуктов, за исключением масла ко-
ровьего, допускается уровень зстрадиола-17бета не более 0.0005 мг/кг
(для масла допускается содержание зстрадиола-17бета не более 0,015 мг/кг.
В случае превышения уровня эстрадиола-17бетта в анализируемом образце бо-
лее,чем на 15%, данный продукт не рекомендуется к употреблению в пищу.
9.АНАЛИТИЧЕСКИЕ ХАРАКТЕРИСТИКИ НАБОРА
9.1. Диапазон измеряемого содержания зстрадиола-17бета составляет
0,1 - 10,0 нг/мл.
9.2. Специфичность анализа. Перекрестная реакция антисыворотки к
зстрадиолу-17бета со структурно-родственными стероидами приведена в таблице 2
Таблица 2
Стероид Перекрестная реакция,%
Эстрадиол-17бета 100
Эстрон 12,0
Эстриол 1,2
Кортизол <0,01
Тестостерон <0,01
5a-Дигидротестостерон <0,01
Прогестерон <0,01
9.3. Минимальное содержание зстрадиола-17бета , определяемое с по-
мощью набора ИФА-АФ- Эстр., составляет 0,06 нг/мл.
9.4. Тест на "линейность". Зависимость содержания зстраднола-17бета
от разведения калибровочных проб находится в диапазоне 85-115 %.
9.5. Воспроизводимость результатов. Коэффициент вариации резуль-
татов измерения содержания зстрадиола-17бета в образцах,полученных с по-
мощью набора ИфА-АФ-Эстр., не превышает 12 %.
9.5. Рекомендуется в каждой лаборатории при использовании набора
ИфА-АФ-Эстр.уточнить значения содержания зстрадиола-17бета, соответствую-
щие нормальным.
10. ПОРЯДОК ПРЕДСТАВЛЕНИЯ РЕКЛАМАЦИЙ
Рекламации на наборы реагентов для количественного определения
зстрадиола в продуктах животного происхождения методом иммунофермент-
ного анализа направляют во Всероссийский государственный научно-иссле-
довательский институт контроля, стандартизации и сертификации ветери-
ных препаратов (ВГНКИ) (123022, г. Москва, Д-22, Звенигородское шоссе,
д.5), предприятию-изготовителю и в Центральную научно-методическую ла-
бораторию (ЦНМВЛ) (111522,г. Москва, улица Оранжерейная, дом 23) в со-
ответствии с указанием ГУБ Минсельхоза России n 22-7/28 от 08.05.92 г.
О порядке предъявления рекламаций на ветпрепараты отечественного
производства и закупаемые по импорту"; одновременно с рекламацией в
адрес ВГНКИ направляют одну тест-систему.
Наставление разработано:
ТОО "М.А.В." (Н.Г.Матрешмна, А.В.Матрешин) и Центральной науч-
но-методической ветеринарной лабораторией (В.А. Седов).
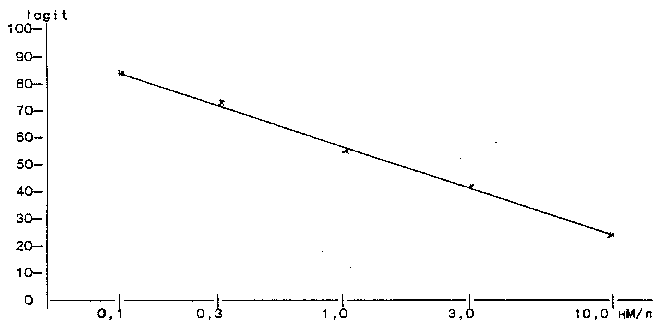 г). Расчет коэффициента выхода гормона (Кв)
Расчет проводится после определения конечных концентраций зстра-
диола-17бета в анализируемых образцах x,y,z (в нг/мл).
y - Х
Кв= ------
z - Х
д). Расчет коэффициента неспецифического влияния компонентов ана-
лизируемых проб на специфическую реакцию связывания зстрадиола-17бета ан-
тителами .
z(нг/мл)
Кнесп. ---------------
5 (нг/мл) + Х
Если Кнесп.> 1 , то это свидетельствует о наличии в образцах сте-
роидов или других соединений, ингибирующих специфическую реакцию.
ПРОДУКТЫ ЖИВОТНОГО ПРОИСХОЖДЕНИЯ, У КОТОРЫХ ЗНАЧЕНИЕ Кнесп ПРЕВЫ-
ШАЕТ 1,15 НЕ РЕКОМЕНДУЕТСЯ УПОТРЕБЛЯТЬ В ПИЩУ ДО ИДЕНТИФИКАЦИИ ОБНАРУ-
ЖЕННЫХ СОЕДИНЕНИЙ; ПРИ ЭТОМ НЕОБХОДИМО ИСКЛЮЧИТЬ НАЛИЧИЕ СТИЛЬБЕНОВ
(ДИЭТИЛСТИЛЬБЭСТРОЛА, ГЕКСОЭСТРОЛА, ДИЕНОЭСТРОЛА) И АНАБОЛИЧЕСКИХ СТЕ-
РОИДОВ (ТРЕНБОЛОНА И 19-НОРТЕСТОСТЕРОНА) В АНАЛИЗИРУЕМЫХ ОБРАЗЦАХ.
е). Расчет истинной концентрации гормона в анализируемом образце
(нг/мл):
Х
Кист. =------------
Кв х К н е с п .
ж). Расчет истинной концентрации гормона в 1 килограмме анализиру-
емого образца (мг/кг):
- Концентрация зстрадиола-17бета в мг/кг мясных продуктов, творога,
сыра расчитывается путем деления полученной величины Кист на 1000.
- Концентрация зстрадиола-17бета в мг/кг масла и жиров животного
происхождения расчитывается путем деления полученной величины Кист на
100.
- Концентрация зстрадиола-17бета в мг/кг молока и кисломолочных про-
дуктов расчитывается путем деления полученной величины Кист на 3000.
ДОПУСТИМЫЕ УРОВНИ ЭСТРАДИОЛА- 17бета
Для всех вышеперечисленных продуктов, за исключением масла ко-
ровьего, допускается уровень зстрадиола-17бета не более 0.0005 мг/кг
(для масла допускается содержание зстрадиола-17бета не более 0,015 мг/кг.
В случае превышения уровня эстрадиола-17бетта в анализируемом образце бо-
лее,чем на 15%, данный продукт не рекомендуется к употреблению в пищу.
9.АНАЛИТИЧЕСКИЕ ХАРАКТЕРИСТИКИ НАБОРА
9.1. Диапазон измеряемого содержания зстрадиола-17бета составляет
0,1 - 10,0 нг/мл.
9.2. Специфичность анализа. Перекрестная реакция антисыворотки к
зстрадиолу-17бета со структурно-родственными стероидами приведена в таблице 2
Таблица 2
Стероид Перекрестная реакция,%
Эстрадиол-17бета 100
Эстрон 12,0
Эстриол 1,2
Кортизол <0,01
Тестостерон <0,01
5a-Дигидротестостерон <0,01
Прогестерон <0,01
9.3. Минимальное содержание зстрадиола-17бета , определяемое с по-
мощью набора ИФА-АФ- Эстр., составляет 0,06 нг/мл.
9.4. Тест на "линейность". Зависимость содержания зстраднола-17бета
от разведения калибровочных проб находится в диапазоне 85-115 %.
9.5. Воспроизводимость результатов. Коэффициент вариации резуль-
татов измерения содержания зстрадиола-17бета в образцах,полученных с по-
мощью набора ИфА-АФ-Эстр., не превышает 12 %.
9.5. Рекомендуется в каждой лаборатории при использовании набора
ИфА-АФ-Эстр.уточнить значения содержания зстрадиола-17бета, соответствую-
щие нормальным.
10. ПОРЯДОК ПРЕДСТАВЛЕНИЯ РЕКЛАМАЦИЙ
Рекламации на наборы реагентов для количественного определения
зстрадиола в продуктах животного происхождения методом иммунофермент-
ного анализа направляют во Всероссийский государственный научно-иссле-
довательский институт контроля, стандартизации и сертификации ветери-
ных препаратов (ВГНКИ) (123022, г. Москва, Д-22, Звенигородское шоссе,
д.5), предприятию-изготовителю и в Центральную научно-методическую ла-
бораторию (ЦНМВЛ) (111522,г. Москва, улица Оранжерейная, дом 23) в со-
ответствии с указанием ГУБ Минсельхоза России n 22-7/28 от 08.05.92 г.
О порядке предъявления рекламаций на ветпрепараты отечественного
производства и закупаемые по импорту"; одновременно с рекламацией в
адрес ВГНКИ направляют одну тест-систему.
Наставление разработано:
ТОО "М.А.В." (Н.Г.Матрешмна, А.В.Матрешин) и Центральной науч-
но-методической ветеринарной лабораторией (В.А. Седов).
г). Расчет коэффициента выхода гормона (Кв)
Расчет проводится после определения конечных концентраций зстра-
диола-17бета в анализируемых образцах x,y,z (в нг/мл).
y - Х
Кв= ------
z - Х
д). Расчет коэффициента неспецифического влияния компонентов ана-
лизируемых проб на специфическую реакцию связывания зстрадиола-17бета ан-
тителами .
z(нг/мл)
Кнесп. ---------------
5 (нг/мл) + Х
Если Кнесп.> 1 , то это свидетельствует о наличии в образцах сте-
роидов или других соединений, ингибирующих специфическую реакцию.
ПРОДУКТЫ ЖИВОТНОГО ПРОИСХОЖДЕНИЯ, У КОТОРЫХ ЗНАЧЕНИЕ Кнесп ПРЕВЫ-
ШАЕТ 1,15 НЕ РЕКОМЕНДУЕТСЯ УПОТРЕБЛЯТЬ В ПИЩУ ДО ИДЕНТИФИКАЦИИ ОБНАРУ-
ЖЕННЫХ СОЕДИНЕНИЙ; ПРИ ЭТОМ НЕОБХОДИМО ИСКЛЮЧИТЬ НАЛИЧИЕ СТИЛЬБЕНОВ
(ДИЭТИЛСТИЛЬБЭСТРОЛА, ГЕКСОЭСТРОЛА, ДИЕНОЭСТРОЛА) И АНАБОЛИЧЕСКИХ СТЕ-
РОИДОВ (ТРЕНБОЛОНА И 19-НОРТЕСТОСТЕРОНА) В АНАЛИЗИРУЕМЫХ ОБРАЗЦАХ.
е). Расчет истинной концентрации гормона в анализируемом образце
(нг/мл):
Х
Кист. =------------
Кв х К н е с п .
ж). Расчет истинной концентрации гормона в 1 килограмме анализиру-
емого образца (мг/кг):
- Концентрация зстрадиола-17бета в мг/кг мясных продуктов, творога,
сыра расчитывается путем деления полученной величины Кист на 1000.
- Концентрация зстрадиола-17бета в мг/кг масла и жиров животного
происхождения расчитывается путем деления полученной величины Кист на
100.
- Концентрация зстрадиола-17бета в мг/кг молока и кисломолочных про-
дуктов расчитывается путем деления полученной величины Кист на 3000.
ДОПУСТИМЫЕ УРОВНИ ЭСТРАДИОЛА- 17бета
Для всех вышеперечисленных продуктов, за исключением масла ко-
ровьего, допускается уровень зстрадиола-17бета не более 0.0005 мг/кг
(для масла допускается содержание зстрадиола-17бета не более 0,015 мг/кг.
В случае превышения уровня эстрадиола-17бетта в анализируемом образце бо-
лее,чем на 15%, данный продукт не рекомендуется к употреблению в пищу.
9.АНАЛИТИЧЕСКИЕ ХАРАКТЕРИСТИКИ НАБОРА
9.1. Диапазон измеряемого содержания зстрадиола-17бета составляет
0,1 - 10,0 нг/мл.
9.2. Специфичность анализа. Перекрестная реакция антисыворотки к
зстрадиолу-17бета со структурно-родственными стероидами приведена в таблице 2
Таблица 2
Стероид Перекрестная реакция,%
Эстрадиол-17бета 100
Эстрон 12,0
Эстриол 1,2
Кортизол <0,01
Тестостерон <0,01
5a-Дигидротестостерон <0,01
Прогестерон <0,01
9.3. Минимальное содержание зстрадиола-17бета , определяемое с по-
мощью набора ИФА-АФ- Эстр., составляет 0,06 нг/мл.
9.4. Тест на "линейность". Зависимость содержания зстраднола-17бета
от разведения калибровочных проб находится в диапазоне 85-115 %.
9.5. Воспроизводимость результатов. Коэффициент вариации резуль-
татов измерения содержания зстрадиола-17бета в образцах,полученных с по-
мощью набора ИфА-АФ-Эстр., не превышает 12 %.
9.5. Рекомендуется в каждой лаборатории при использовании набора
ИфА-АФ-Эстр.уточнить значения содержания зстрадиола-17бета, соответствую-
щие нормальным.
10. ПОРЯДОК ПРЕДСТАВЛЕНИЯ РЕКЛАМАЦИЙ
Рекламации на наборы реагентов для количественного определения
зстрадиола в продуктах животного происхождения методом иммунофермент-
ного анализа направляют во Всероссийский государственный научно-иссле-
довательский институт контроля, стандартизации и сертификации ветери-
ных препаратов (ВГНКИ) (123022, г. Москва, Д-22, Звенигородское шоссе,
д.5), предприятию-изготовителю и в Центральную научно-методическую ла-
бораторию (ЦНМВЛ) (111522,г. Москва, улица Оранжерейная, дом 23) в со-
ответствии с указанием ГУБ Минсельхоза России n 22-7/28 от 08.05.92 г.
О порядке предъявления рекламаций на ветпрепараты отечественного
производства и закупаемые по импорту"; одновременно с рекламацией в
адрес ВГНКИ направляют одну тест-систему.
Наставление разработано:
ТОО "М.А.В." (Н.Г.Матрешмна, А.В.Матрешин) и Центральной науч-
но-методической ветеринарной лабораторией (В.А. Седов).