Наставление
по применению набора компонентов
для диагностики бешенства
животных в реакции диффузионной преципитации
1. Общие сведения
2. Подготовка материалов.
3. Постановка реакции.
4. Учет и оценка результатов.
5. Предъявление рекламации.
МИНИСТЕРСТВО
cЕЛЬСКОГО ХОЗЯЙСТВА
И ПРОДОВОЛЬСТВИЯ
РОССИЙСКОЙ ФЕДЕРАЦИИ
(Минсельхозпрод России)
УТВЕРЖДАЮ
ДЕПАРТАМЕНТ ВЕТЕРИНАРИИ Заместитель руководителя
Департамента ветеринарии
25.06.1999г. № 13-7-2/1662 В.В.Селиверстов
НАСТАВЛЕНИЕ
по применению набора компонентов
для диагностики бешенства
животных в реакции диффузион-
ной преципитации
1. Общие сведения
1.1. Набор компонентов для диагностики бешенства в реакции диффу-
зионной преципитации (РДП) предназначен для выявления вируса бешенства
в головном мозге животных.
1.2. Набор состоит из следующих компонентов:
- сыворотка преципитирующая - 4 ампулы по 1,5 куб.см, сухая пористая
масса белого цвета с сероватым оттенком;
- антиген положительный - 4 ампулы по 0,5 куб.см, сухая пористая
масса светло-серого или светло-коричневого цвета;
- антиген отрицательный - 2 ампулы по 1,0 куб.см, сухая пористая
масса белого цвета с сероватым оттенком.
1.3. Компоненты набора уложены в картонные коробки с разделитель-
ными перегородками, обеспечивающими неподвижность ампул.
1.4. На этикетке ампулы должны быть указаны: наименование компо-
нента, объем, номер серии, дата изготовления. На коробке должна быть
этикетка с указанием предприятия-изготовителя и его товарного знака,
наименования набора, наименования компонентов набора и их количества,
номера серии и контроля, даты изготовления, срока годности, условии
хранения, обозначения ТУ.
1.5. Диагностикум хранят в сухом темном месте при температуре
2-4°С. Срок годности 12 мес. при соблюдении условий хранения.
1.6. При изменении цвета, консистенции или плохой растворимости
компонентов применение набора прекращают. Ампулы, содержащее плесень,
посторонние примеси, а также с нарушением целостности, без этикетки
бракуют.
2.Подготовка материалов.
2.1.Приготовление агарового геля.
Агаровый 1,5% гель готовят по прописи:
- агар - 15 г;
- метиловый оранжевый - 0,03 г;
- мертиолат - 0,01 г;
- хлористый натрий - 8,5 г;
- вода дистиллированная - 1 куб.дм.
Используют отар "Дифко" (США) или любой другой высокой степени
Очистки. Агар растворяют при нагревании до 80-90 гр.С и добавляют осталь-
ные реактивы по прописи. Готовый агар разливают по 30-50 куб.см во флако-
ны и хранят при температуре 2-6 гр.С в течение месяца. Перед использова-
нием агар расплавляют в кипящей водяной бане.
2.2. Подготовка компонентов набора.
В ампулу с сывороткой преципитирующей вносят 1,5 куб.см физиологи-
ческого растворам при этом содержимое ампулы должно полностью раство-
риться в течение 4 мин. с образованием прозрачной слегка опалесцирующей
жидкости. Далее делают двукратные разведения 1:2, 1:4, 1:8, 1:16.
В ампулы с антигеном положительным и антигеном отрицательным вно-
сят физиологический раствор в объеме, указанном на этикетке. Содержи-
мое ампул должно раствориться в течение 30 мин. с образованием гомоген-
ной взвеси светло-серого или светло-коричневого цвета, которую исполь-
зуют в качестве положительного и отрицательного контролей.
Растворенные сыворотка преципитирующая и антиген отрицательный
пригодны в течение 15 дн., антиген положительный - в течение 3 дн. при
условии хранения их плотно закрытыми при температуре 2-4°С.
2.3. Подготовка исследуемых материалов.
У крупных животных, собак, кошек исследуют следующее отделы го-
доеного мозга: кору полушарий, аммонов рог, мозжечок и продолговатый
мозг. Кусочки мозга из коры полушарий, аммонова рога, мозжечка, про-
долговатого мозга (каждый по отдельности) растирают в ступке до обра-
зования однородной массы и исследуют отдельно. От мышей исследуют весь
головной мозг.
Для постановки РДП пригоден как свежий мозг, так и мозг на на-
чальной стадии разложения. Мозговая ткань, консервированная глицери-
ном, формалином, ацетоном и спиртом, не пригодна для исследования в
РДП.
3.Постановка реакции.
3.1. Реакцию ставят в чашках Петри или на предметных стеклах. В
чашки Петри наливают по 10 куб.см, на предметные стекла - по 3 куб.см
расп-
лавленного агара и дают застыть на горизонтальной поверхности. После
застывания среда должна быть совершенно гомогенной и прозрачной и не
содержать никаких частиц.
В пластинке отара с помощью тонкостенной металлической трубочки
диаметром 5 мм делают розетку из 4-х лунок, расположенных вокруг одном
центральной лунки на расстоянии 5 мм, по трафарету, который подклады-
вают под дно чашки Петри или под стекло, в чашке Петри располагают
4 розетки, на предметном стекле - 2 розетки.
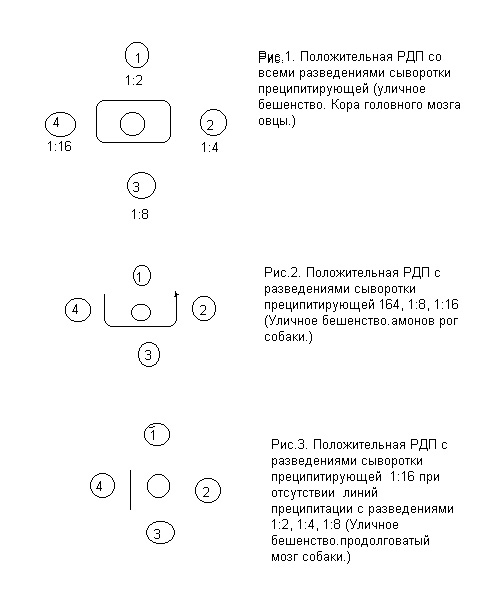
3.2. Лунки, обозначенные цифрами 1, 2, 3, 4 (рис. 1), заполняют
сывороткой преципитирующей в разведениях 1:2, 1:4, 1:8, 1:16.
3.3. В центральную лунку вносят каплю исследуемого мозга животных
с подозрением на бешенство. Одновременно ставят контроли с положитель-
ным и отрицательным антигенами из набора, но каждый в отдельной чашке
или на отдельном стекле.
3.4. Чашки Петри или предметные стекла переносят во влажную каме-
ру и ставят в термостат (37±1°С) на 12 ч. Затем чашки оставляют при
температуре 20-25°С на 80 ч. По мере диффузии препаратов в отар в лун-
ки с сывороткой подкапывают сыворотку преципитирующую, а в лунки с
исследуемым материалом и контрольными антигенами - стерильный физиоло-
гический раствор, чтобы они не оставались пустыми.
4. Учет и оценка результатов.
4.1. Учет результатов реакции проводят через 12, 24, 48 и 72 ч.
после ее постановки. Линии преципитации видимы визуально в проходящем
свете при просвечивании осветлителем снизу вверх. Вирус бешенства обра-
зует с сывороткой преципитирующей одну или две линии преципитации.
4.2. Учет результатов начинают о просмотра розеток с контрольными
антигенами. Сыворотка преципитирующая должна образовывать линии преци-
питации с антигеном положительным и не образовывать - с антигеном от-
рицательным.
4.3. С исследуемым материалом линии преципитации могут образовы-
ваться вокруг лунки с антигеном как со всеми разведениями сыворотки
преципитирующей, так и с одним из разведений (рис. 1, 2, 3). Реакция
может быть положительной с материалом как из некоторых отделов мозга,
так и с материалом из всех отделов мозга.
 4.2.Для постановки положительного диагноза на бешенство доста-
точно образования линии преципитации с материалом хотя бы из одного
отдела головного мозга.
В случае отсутствия линии преципитации между лунками с сывороткой
преципитирующей и исследуема материалом результат реакции считают от-
рицательным.
4.5. При получении отрицательного результата ставят биопробу (с
материалом, не подвергшиеся разложению) на белых мышах или кроликах в
соответствии с "Методическими указаниями" по лабораторной диагностике
бешенства", утвержденными 27.02.70г.
4.4. Материалы, содержащие вирус бешенства и контаминированные
вирусом инструменты и посуду автоклавируют в течение 1ч. при 1,5 атм.
5. Предъявление рекламации.
В случае выявления неактивности препарата или неспецифической ре-
акции его применение прекращают и в соответствии с указанием
ГУБ МСХ РФ от 08.05.92г., № 22-7/28 "О порядке предъявления рекламаций
на ветпрепараты отечественного производства и закупаемые по импорту"
сообщают Всероссийскому государственному научно-исследовательскому
институту контроля, стандартизации и сертификации ветеринарных препа-
ратов (ВГНКИ, 123022, Москва, Звенигородское шоссе,5), предприя-
тию-изготовителю (ВНИиТИБП, 141142, Московская обл., Щелковский р-он,
п/о Кашинцево), Центральной научно-методической ветеринарной лаборато-
рии (ЦНМВЛ, 111622, Москва, ул.Оранжерейная,23).
Одновременно при наличии невскрытые наборов один упаковывают,
опечатывают и направляют с нарочным или почтой во ВГНКИ.
Наставление разработано ВНИиТИБП .
Расссмотрено и рекомендовано к применению и регистрации в
Российской Федерации Советом по ветеринарным препаратам 23.04.99г.
(протокол № 2)
ПВР-1-2.9 /00074.
4.2.Для постановки положительного диагноза на бешенство доста-
точно образования линии преципитации с материалом хотя бы из одного
отдела головного мозга.
В случае отсутствия линии преципитации между лунками с сывороткой
преципитирующей и исследуема материалом результат реакции считают от-
рицательным.
4.5. При получении отрицательного результата ставят биопробу (с
материалом, не подвергшиеся разложению) на белых мышах или кроликах в
соответствии с "Методическими указаниями" по лабораторной диагностике
бешенства", утвержденными 27.02.70г.
4.4. Материалы, содержащие вирус бешенства и контаминированные
вирусом инструменты и посуду автоклавируют в течение 1ч. при 1,5 атм.
5. Предъявление рекламации.
В случае выявления неактивности препарата или неспецифической ре-
акции его применение прекращают и в соответствии с указанием
ГУБ МСХ РФ от 08.05.92г., № 22-7/28 "О порядке предъявления рекламаций
на ветпрепараты отечественного производства и закупаемые по импорту"
сообщают Всероссийскому государственному научно-исследовательскому
институту контроля, стандартизации и сертификации ветеринарных препа-
ратов (ВГНКИ, 123022, Москва, Звенигородское шоссе,5), предприя-
тию-изготовителю (ВНИиТИБП, 141142, Московская обл., Щелковский р-он,
п/о Кашинцево), Центральной научно-методической ветеринарной лаборато-
рии (ЦНМВЛ, 111622, Москва, ул.Оранжерейная,23).
Одновременно при наличии невскрытые наборов один упаковывают,
опечатывают и направляют с нарочным или почтой во ВГНКИ.
Наставление разработано ВНИиТИБП .
Расссмотрено и рекомендовано к применению и регистрации в
Российской Федерации Советом по ветеринарным препаратам 23.04.99г.
(протокол № 2)
ПВР-1-2.9 /00074.
 4.2.Для постановки положительного диагноза на бешенство доста-
точно образования линии преципитации с материалом хотя бы из одного
отдела головного мозга.
В случае отсутствия линии преципитации между лунками с сывороткой
преципитирующей и исследуема материалом результат реакции считают от-
рицательным.
4.5. При получении отрицательного результата ставят биопробу (с
материалом, не подвергшиеся разложению) на белых мышах или кроликах в
соответствии с "Методическими указаниями" по лабораторной диагностике
бешенства", утвержденными 27.02.70г.
4.4. Материалы, содержащие вирус бешенства и контаминированные
вирусом инструменты и посуду автоклавируют в течение 1ч. при 1,5 атм.
5. Предъявление рекламации.
В случае выявления неактивности препарата или неспецифической ре-
акции его применение прекращают и в соответствии с указанием
ГУБ МСХ РФ от 08.05.92г., № 22-7/28 "О порядке предъявления рекламаций
на ветпрепараты отечественного производства и закупаемые по импорту"
сообщают Всероссийскому государственному научно-исследовательскому
институту контроля, стандартизации и сертификации ветеринарных препа-
ратов (ВГНКИ, 123022, Москва, Звенигородское шоссе,5), предприя-
тию-изготовителю (ВНИиТИБП, 141142, Московская обл., Щелковский р-он,
п/о Кашинцево), Центральной научно-методической ветеринарной лаборато-
рии (ЦНМВЛ, 111622, Москва, ул.Оранжерейная,23).
Одновременно при наличии невскрытые наборов один упаковывают,
опечатывают и направляют с нарочным или почтой во ВГНКИ.
Наставление разработано ВНИиТИБП .
Расссмотрено и рекомендовано к применению и регистрации в
Российской Федерации Советом по ветеринарным препаратам 23.04.99г.
(протокол № 2)
ПВР-1-2.9 /00074.
4.2.Для постановки положительного диагноза на бешенство доста-
точно образования линии преципитации с материалом хотя бы из одного
отдела головного мозга.
В случае отсутствия линии преципитации между лунками с сывороткой
преципитирующей и исследуема материалом результат реакции считают от-
рицательным.
4.5. При получении отрицательного результата ставят биопробу (с
материалом, не подвергшиеся разложению) на белых мышах или кроликах в
соответствии с "Методическими указаниями" по лабораторной диагностике
бешенства", утвержденными 27.02.70г.
4.4. Материалы, содержащие вирус бешенства и контаминированные
вирусом инструменты и посуду автоклавируют в течение 1ч. при 1,5 атм.
5. Предъявление рекламации.
В случае выявления неактивности препарата или неспецифической ре-
акции его применение прекращают и в соответствии с указанием
ГУБ МСХ РФ от 08.05.92г., № 22-7/28 "О порядке предъявления рекламаций
на ветпрепараты отечественного производства и закупаемые по импорту"
сообщают Всероссийскому государственному научно-исследовательскому
институту контроля, стандартизации и сертификации ветеринарных препа-
ратов (ВГНКИ, 123022, Москва, Звенигородское шоссе,5), предприя-
тию-изготовителю (ВНИиТИБП, 141142, Московская обл., Щелковский р-он,
п/о Кашинцево), Центральной научно-методической ветеринарной лаборато-
рии (ЦНМВЛ, 111622, Москва, ул.Оранжерейная,23).
Одновременно при наличии невскрытые наборов один упаковывают,
опечатывают и направляют с нарочным или почтой во ВГНКИ.
Наставление разработано ВНИиТИБП .
Расссмотрено и рекомендовано к применению и регистрации в
Российской Федерации Советом по ветеринарным препаратам 23.04.99г.
(протокол № 2)
ПВР-1-2.9 /00074.